دانستنیهایی درباره یون هالید به عناصر گروه ۱۷ جدول تناوبی که دارای ۷ الکترون در لایه ظرفیت خود هستند، اصطلاحاً هالوژن گفته میشود. این عناصر با دریافت یک الکترون به آرایش هشتایی و پایدار رسیده و یون هالید را تشکیل میدهند. حالا از چه طریقی بفهمیم که یون هالید تشکیل شده است؟
روشهای مختلفی برای این کار وجود دارد. یکی از این روشها قابلیت حلالیت در آب است. به عبارت بهتر یون هالید توانایی حل شدن در آب و تشکیل رسوب را دارد.
در این مقاله از پارسیان شیمی طهران همراه ما باشید تا اطلاعات دقیقتری درباره یون هالید و تأثیر آن در صنایع مختلف به شما ارائه دهیم.
یون هالید چیست
هالوژنها معمولاً در ترکیبهای متنوع به صورت هالید ظاهر میشوند تا بتوانند با ذرات دیگر در پیوندهای شیمیایی شرکت کنند. در ادامه برخی از هالیدهای رایج جدول تناوبی به شما معرفی میشوند:
- یدید؛
- استاتید؛
- برمید؛
- فلوئورید؛
از میان یونهای هالید نام برده شده، استاتید خاصیت پرتوزایی و رادیواکتیو دارد. اما سؤال اصلی این است که یونهای هالید چه خواصی دارند؟ در بخش بعدی همراه ما باشید تا به این سؤال شما پاسخ دهیم.
مهمترین خواص یونهای هالید
یونهای هالید معمولاً به عنوان یک عامل کاهنده عمل کرده و با از دست دادن بیرونیترین لایه الکترون خود با عناصر مختلف جدول تناوبی ترکیب میشوند. به عبارت بهتر یونهایی که در پایین گروه ۱۷ جدول تناوبی قرار دارند، الکترون خود را راحتتر از بقیه عناصر از دست میدهند.
تأثیر قرص لسیتین در درمان بیماریها
ترکیبات مختلف یونهای هالید
شاید برایتان جالب باشد که بدانید یونهای هالید با چه عناصری ترکیب شده و چه موادی را تشکیل میدهند. این یونها به راحتی با عناصر گروههای مختلف جدول تناوبی واکنش داده و عناصر جدید میسازند. مثلاً فلزات قلیایی میتوانند با یونهای هالید ترکیب شده و عناصری با خواص جدید تشکیل دهند.
ترکیب یونهای هالید با فلزات قلیایی
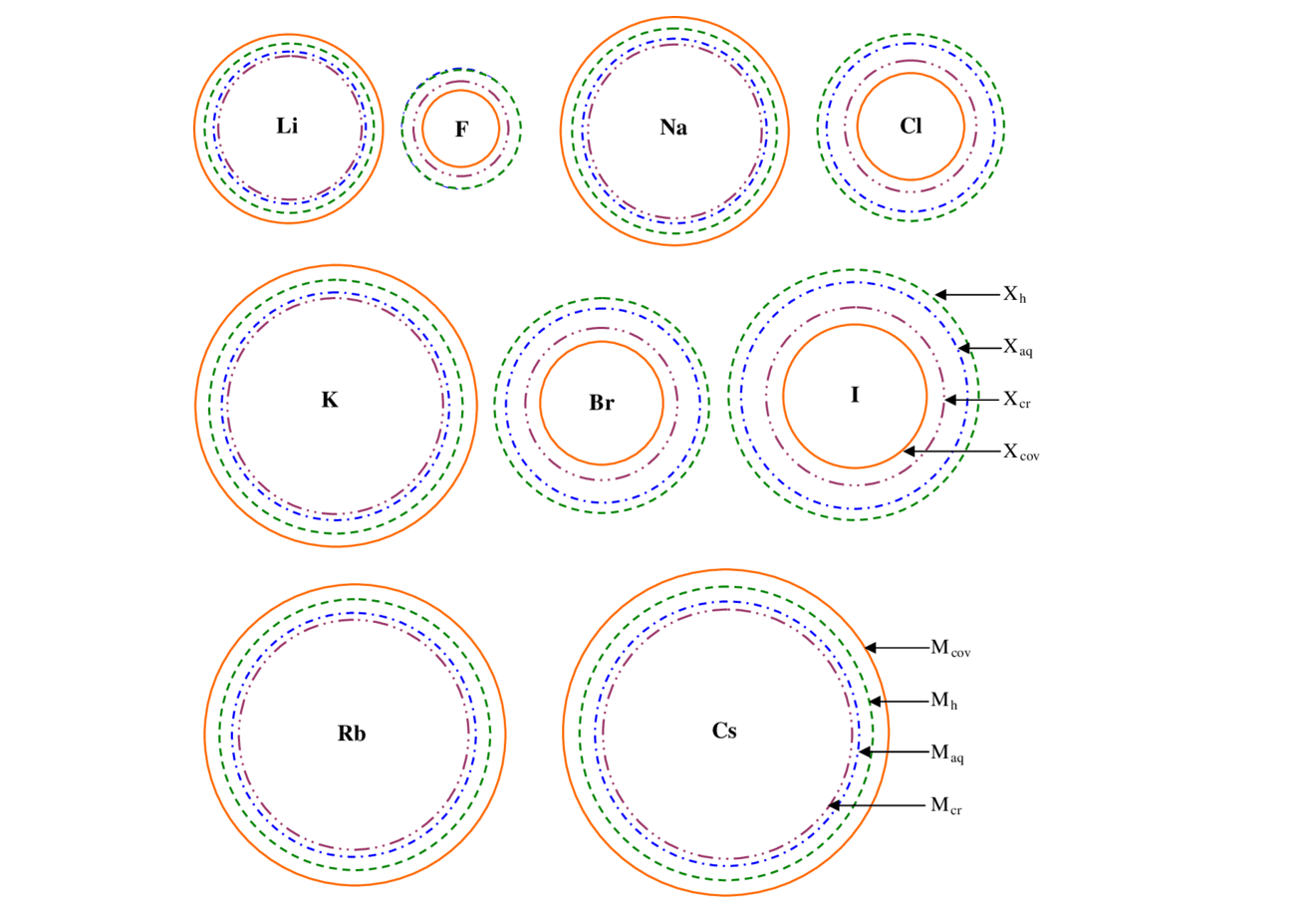
زمانی که یونهای هالید با فلزات قلیایی ترکیب میشوند، جامدهای کریستالی تشکیل میدهند که اصطلاحاً هالید فلزات قلیایی خوانده میشوند. این عناصر نقطه ذوب بسیار بالایی داشته و به راحتی در آب حل میشوند. در این میان تنها لیتیم فلوئورید است که به راحتی در آب حل نشده و دلیل این موضوع کوچک بودن اندازه آنیون و کاتیون آن است.
یونهای هالید دیگر مثل لیتیم کلرید در اتیل استات، استون یا اتانول به راحتی حل میشوند. انحلالپذیری سزیم یدید به دلیل کم بودن انرژی هیدراته آنها بسیار پایینتر از بقیه عناصر است.
مهمترین ترکیبات فلزات قلیایی خاکی با دانستنیهایی درباره یون هالید
از بین ترکیبات فلزات قلیایی با یون هالید، برلیوم کلرید و منیزیم کلرید میتوانند در حلالهای آلی به راحتی حل شوند. میزان حل شدن این عناصر گروه جدول تناوبی در آب بسیار کم بوده اما برخی ترکیبات آنها می توانند در آب حل شوند.
ترکیب یون هالید با هیدروژن
ترکیب یون هالید با هیدروژن کاربردهای زیادی در صنایع مختلف دارد. این ترکیبات نقش اسیدی بسیار قوی داشته در حالی که هیدروژن فلوئورید مانند یک اسید ضعیف عمل میکند.
شما میتوانید در آزمایشگاهها به راحتی یونهای هالید را با اسیدهای فرار به دست بیاورید.
نکته جالب توجه اینکه زمانی که یونهای هالید با عناصر مختلف جدول تناوبی ترکیب میشوند، رسوب برخی از آنها دارای رنگ های متنوعی است. مثلاً رسوب کلرید دارای رنگ سفید یا رسوب برمید دارای رنگ زرد روشن است.
در مقاله دانستنیهایی درباره یون هالید از پارسیان شیمی طهران سعی کردیم اطلاعات مفیدی درباره یون هالید، چگونگی تشکیل آن و کاربردهای این یون در صنایع مختلف در اختیار شما قرار دهیم. شما میتوانید نظرات خود را از طریق بخش دیدگاههای همین صفحه با ما و دوستانتان به اشتراک بگذارید.